Covid-19 Autorisation de mise sur le marché de médicaments à la Pfizer – ce qui ne convient pas est adapté!
#Blotgate, une nouvelle dimension de la fraude intentionnelle
Face à l’inflation d’informations sur les agissements criminels dans le contexte de la production et de l’utilisation des injections expérimentales de thérapie génique avec les principes actifs recombinants du Covid-19 (« vaccin SARS-CoV-2 ou Corona », voir [A]), un article remarquable [1] de la journaliste d’investigation britannique Sonja Elijha [2] est presque passé inaperçu. Pourtant, les résultats des recherches minutieuses de cette ancienne chercheuse de la BBC pourraient bien avoir le potentiel de changer la donne dans le traitement juridique et la condamnation des responsables de ce qui est probablement la plus grande fraude scientifique et le plus grand scandale médical de l’histoire de l’humanité. Dans les cercles spécialisés, cette publication d’Elijah fait l’objet d’un débat approfondi et d’une évaluation professionnelle sous le mot-clé #blotgate [3].
Elijah avait déjà rendu d’énormes services en analysant les documents et la correspondance de Pfizer dans le cadre des phases d’essais cliniques télescopiques [4]. Elle avait effectué exactement les tests qui sont en fait destinés aux départements spécialisés des autorités d’autorisation de mise sur le marché auprès de l’EMA (European Medicines Agency/Agence européenne des médicaments) ou de la FDA (US Food and Drug Administration). Selon l’état actuel des connaissances, ces autorités, tout comme au niveau national selon le §22 de l’AMG (loi sur les médicaments) le BfARM (Institut fédéral des médicaments et des dispositifs médicaux), le PEI (Institut Paul Ehrlich) et l’IQWiG (Institut pour la qualité et l’efficacité économique dans le système de santé), ainsi que les processus d’évaluation par les pairs dans les revues scientifiques spécialisées concernées [5] ont totalement échoué sur toute la ligne. Un tel échec structurel ne peut s’expliquer ni par la négligence ni par le hasard, mais probablement par une entente délibérée et ciblée en vue d’une fraude. Cela n’a rien d’étonnant avec l’entrée dans l’ère de la dépendance aux fonds de tiers et du funeste partenariat public-privé. Ces changements fondamentaux dans la recherche, auparavant indépendante et financée par les impôts, ont transformé des institutions scientifiques autrefois largement neutres et objectives en instituts de recherche sous contrat, de corruption industrielle et d’expertise de complaisance. Cela a également permis à l’industrie pharmaceutique de financer essentiellement les autorités de régulation qu’elle est censée contrôler [6]. Ils ont même réussi à placer une lobbyiste pharmaceutique (Emer Cooke) à la tête de l’EMA en novembre 2020, juste avant l’octroi de la première autorisation de mise sur le marché conditionnelle du Covid-19 en décembre 2020 [7], ce qui est malhonnête.
Un bref récapitulatif de ce qui a pu être établi jusqu’à présent facilite la compréhension des relations tout à fait complexes de biologie moléculaire et d’analyse instrumentale qui sont à la base des nouveaux résultats de l’enquête d’Elijah.
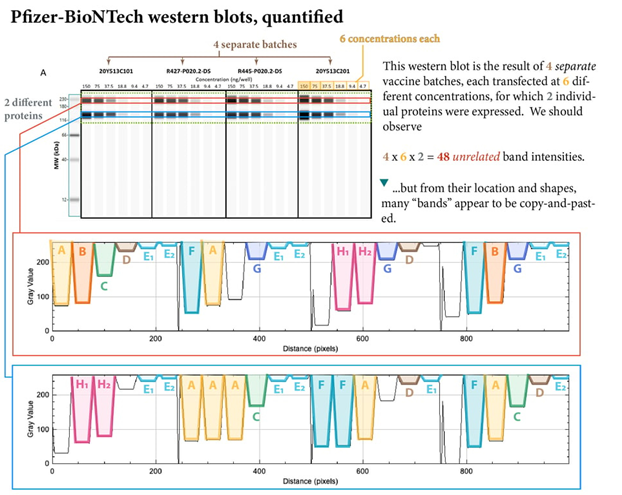
En janvier 2021 déjà, la biologiste cellulaire Dr Vanessa Schmidt-Krüger avait analysé le rapport d’évaluation ouvert de l’EMA sur Corminaty (le « vaccin » de thérapie génique Covid-19 de Pfizer/BioNTech) [8, 34]. L’un des points essentiels de leur critique concernait le manque total de clarté de la composition du produit final issu de la fabrication industrielle à grande échelle, ce que les examinateurs de l’EMA avaient tout de même également remarqué. La constatation que, contrairement à la documentation de l’intégrité de l’ARNm (une mesure de pureté qui indique la quantité d’ARNm entièrement intact contenue dans les échantillons) à l’échelle du laboratoire, l’intégrité de l’ARNm dans les études cliniques était de 78%, contre 55% dans la production industrielle de masse, a été déterminante. Le modRNA intact se caractérise par une structure initiale dite de cap 5, la séquence de nucléotides codant pour la protéine à traduire (dans ce cas, la protéine spike du SRAS-CoV-2) et une queue poly-A dite finale de 3. De plus, l’ARNm original du SRAS-CoV-2 (ARN messager [9]) a été modifié dans la substance active (Tozinameran) de Comirnaty par le remplacement de la base nucléique uracile par de la pseudouridine (d’où modRNA [10]) afin de réduire la réactogénicité. Dans la séquence codante, une protéine d’ancrage membranaire est ajoutée, ce qui empêche la formation de protéines de pointe libres circulant dans le système cardiovasculaire, ainsi qu’une protéine de verrouillage (2P Lock), qui devrait empêcher le clivage (sur le site de clivage de la furine) et l’ouverture des sites de liaison de la sous-unité S1 [11]. Ces deux dernières modifications se sont entre-temps révélées inefficaces, de sorte que les protéines spike circulant librement dans le cocktail toxique de Pfizer peuvent déployer pleinement leurs propriétés toxiques connues dans l’organisme. La diminution de l’intégrité du modRNA, critiquée par les auditeurs de l’EMA, comporte un énorme potentiel de risque pour les patients. Une analyse différenciée de l’infusion provenant des cuves pharmaceutiques de Pfizer a révélé la présence d’ARNm fragmentés (appelés truncated s.a. [1(a), 3] #humpgate), dont personne ne sait ce qu’ils expriment éventuellement comme protéines étrangères, de composants résiduels d’ADN linéarisé et de diverses enzymes issues du processus de synthèse de l’ARNm, ainsi que d’autres impuretés microbiologiques [B]. En outre, on peut se demander dans quelle mesure la teneur réduite en substance active peut encore avoir l’effet postulé (réaction immunitaire et formation d’anticorps). Les examinateurs de l’EMA ont donc tout de même posé une question clé qui aurait dû trouver une réponse concluante dans le dossier d’autorisation. La preuve expérimentale demandée par l’EMA pour la vérification du produit final, entre autres par l’analyse Western Blot [12], revêt donc une importance essentielle pour la sécurité des consommateurs.